Termoquímica
Um dos conteúdos que assustam no Ensino Médio. Vamos descomplicar?
O que é?
Ramo da Química que estuda a energia em movimento de processos químicos em mudanças de fase ou em reações, e como ela pode ser transferida de um lugar ao outro.
Calor: o que é e como medir?
O calor pode ser definido como a energia que flui de um corpo para outro quando estes têm temperaturas diferentes. Essa transição sempre se dá do corpo mais quente para o mais frio.
O calor já foi considerado uma substância. Mas não é. Ele é produto do contato de corpos cuja agitação de moléculas é maior ou menor, gerando um fluxo de energia.
Saiba mais: Lei Zero e Primeira lei da Termodinâmica.
É importante, para seguirmos adiante, saber a diferença entre calor e energia térmica. Calor é uma energia em movimento decorrente da diferença de temperatura. Já a energia térmica é a energia associada ao movimento desordenado de moléculas para temperaturas acima do zero absoluto.
A unidade conveniente
para medir isso é a caloria (representada por cal). Ela equivale à energia necessária para elevar em 1 °C a temperatura de
1 g de água. Para tudo é necessário um padrão e, para medir a caloria, esse
foi o padrão escolhido. Outra unidade, mais usada na Física para definir o
trabalho exercido por uma força de 1 newton por um metro. É o tal do joule,
representado por J.
Experiências realizadas permitiram estabelecer uma relação entre a caloria e o joule. Vale a pena lembrar desse número aqui:
1 cal = 4,18 J
Para fazer essa conversão, basta usar uma regra de três. Comumente, também, é usado o quilojoule (kJ), que corresponde a 1.000 joules
Entalpia e entropia
Entropia é um conceito que não será muito explorado. Por enquanto, podemos entender a entropia como a desordem de um sistema.
A entalpia é uma grandeza (expressa em unidade de energia) informa quanta quantidade de energia em um sistema poderia ser transformada em calor quando submetido a um processo de pressão constante.
A variação de entalpia de um sistema informa a quantidade de calor trocado pelo sistema. A partir disso podemos saber se um processo é exotérmico (ou seja, libera calor) ou endotérmico.
A entalpia é afetada pela temperatura, pressão e estado físico.
A variação de entalpia, ΔH, é a definida como a variação da energia do sistema, ou:
ΔH = Hf (final da reação) - Hi (início da reação)
Por essa equação, temos que, quando ΔH < 0, o processo é exotérmico e, portanto, libera energia. Para ΔH > 0, o processo é endotérmico e, portanto, absorve energia.
A variação de entalpia é bastante usada para representar mudanças de fases. Por exemplo, quando a água passa do estado líquido para o sólido, há uma perda de 6,01 k J. Portanto, a variação da entalpia é de - 6,01 kJ. O processo inverso, quando a água passa do estado sólido para líquido, tem uma entalpia de +6,01 kJ, indicando a perda de energia. Nessas situações, o sinal negativo indica um processo exotérmico e o sinal positivo, um processo endotérmica.
Vale lembrar que, para uma reação
que pode ocorrer no sentido direto e no sentido inverso, a entalpia será a
mesma, mas é necessário cuidar o sinal: se a reação direta for exotérmica (ΔH
negativo), a reação inversa será endotérmica (ΔH positivo), e vice-versa.
Processos exotérmicos
Essas reações liberam calor, formando produtos com energia menor do que a dos reagentes. São as reações termodinamicamente mais estáveis e, também, geralmente, as mais espontâneas. Podemos nos encontrar com um gráfico para a variação de entalpia.
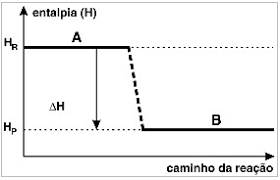
Processos endotérmicos:
Essas reações absorvem calor, formando produtos com mais energia que os reagentes. O gráfico desse processo é:
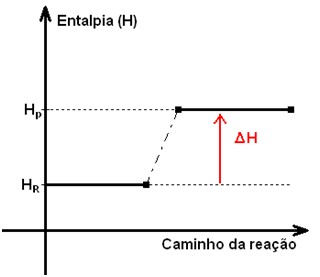
Estado padrão de entalpia:
O estado padrão de entalpia é o valor da variação de entalpia para 1 mol de substância em condições padrões, como:
- Estado físico mais comum.
- Estado alotrópico mais estável.*
- 25 °C
- 1 atm de pressão
Substâncias simples nesse estado padrão tem entalpia igual a zero. Exemplo: a entalpia do O2 e do H2 é zero, no estado padrão, e esse valor é simbolizado por ΔH°.
*Aqui é bom prestar atenção, pois temos cinco elementos que merecem o destaque: COSP (carbono, oxigênio, enxofre e fósforo).
Fique atento! Não confunda CNTP e condições ambiente: na CNTP, temos uma temperatura de 0 °C e pressão de 1 atm, já as condições ambientes são 25 °C e 1 atm (usado para definir o estado padrão de entalpia.
Energia de ativação e complexo ativado
A energia de ativação é definida como a energia mínima necessária para que aconteça a reação. Já o complexo ativado é um "meio termo" entre a transformação de reagentes e produtos. Nessa fase, existem ligações enfraquecidas (no caso dos reagentes) e a formação de ligações (no caso dos produtos). A melhor maneira de visualizar isso é através do gráfico:
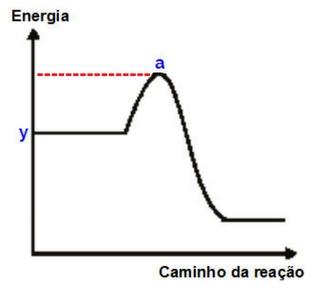
Em que "a" é o complexo ativado e a distância vertical entre "y" e "a" corresponde à energia de ativação.
Como calcular a energia de ativação? Basta subtrair a energia do complexo ativado pela energia dos reagentes (nesse caso, indicada por "y").
Energia de ativação = H (do complexo ativado) - H (reagentes)
Com base nesse gráfico, vemos que:
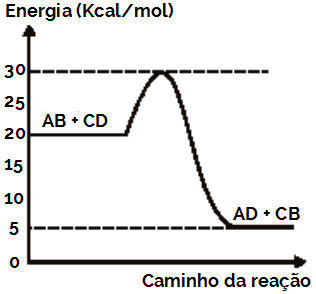
A energia do complexo ativado tem valor de 30 kcal/mol. A energia dos reagentes e dos produtos são, respectivamente, 20 kcal/mol e 5 kcal/mol. A energia de ativação é 10 kcal, pois:
H complexo ativado = 30
H reagentes= 20
Energia de ativação = H(complexo ativado) - H(reagentes)
Energia de ativação = 30 kcal - 20 kcal = 10 kcal
Tipos de variação de entalpia:
- Entalpia de formação: é a energia envolvida na formação de 1 mol de substância. A equação química da entalpia de formação tem um só produto com coeficiente estequiométrico igual a 1. Exemplo: H2 + ½ O2 -> H2O.
- Entalpia de combustão: energia envolvida no processo de queima de um combustível. Genericamente, pode ser escrita assim: Combustível + O2 -> energia. Nas reações de combustão completa, os produtos são CO2 e H2O. Nas reações de combustão incompleta, os produtos são CO e fuligem (C).
- Entalpia padrão de combustão: combustão completa de 1 mol de certa substância sob pressão constante.
- Entalpia de ligação: energia absorvida na quebra das ligações entre os átomos de determinada molécula ou energia liberada na formação de uma nova molécula. Essa entalpia será importante para os cálculos mais adiante.
Exemplo: 2 H (g) -> H2 (g) ΔH = - 436 kJ/mol (formação)
H2 (g) -> 2 H (g) ΔH = + 436 kJ/mol (quebra)
- Entalpia de neutralização: variação de energia que ocorre durante um processo de neutralização de um ácido por uma base ou vice-versa.
Exemplo: HCl + NaOH -> Na^+ (aq) + Cl^- (aq) + H2O (l) ΔH°= - 57,7 kJ/mol
Importante: a neutralização entre ácidos fortes e bases fortes ocorre com a mesma liberação de energia, já que o produto formado é o mesmo (H2O).
- Entalpia de dissolução: variação de entalpia envolvida na dissolução de uma substância nas condições padrão. A separação das partículas de um soluto é um processo endotérmico. A hidratação das partículas de um soluto é exotérmica
Métodos de cálculo de variação de entalpia e quando usá-los
Agora vamos ver qual fórmula usar (e quando usar) na hora de calcular, de fato, a entalpia.
- Pela fórmula ΔH = H (dos produtos) - H (reagentes)
- Pela enérgica de ligação
Esse método é o mais simples. Mas fique atento: você só vai poder aplicar ele se nas questões forem dadas as entalpias de formação! Lembrando que, para substância simples no estado padrão de entalpia, ΔH é zero. Aqui, o sinal de cada entalpia será analisado no final. Para explicar esse método, vamos resolver um problema. Calcule a variação de entalpia da seguinte equação: C3H8 (g) + O2 (g) -> CO2 (g) + H2O (l). Dados:
H formação C3H8 (g) = -47 kcal/mol
H formação H2O (l) = - 68 kcal/mol
H formação CO2 (g) = -94 kcal/mol
Lembre-se: a entalpia de formação vale para 1 MOL da substância.
Primeiro passo: balancear a equação
1 C3H8 (g) + 5 O2 (g) = 3 CO2 (g) + 4 H2O (l)
Segundo passo: separar os reagentes e os produtos
Reagentes: 1 C3H8 (g) e 5 O2 (g)
Produtos: 3 CO2 (g) e 4 H2O (l)
Terceiro passo: calcular a entalpia dos reagentes e dos produtos
Regentes:
1 x C3H8 (g) = 1 x -47 = -47 kcal/mol
5 x O2 (g) = 5 x 0 = o kcal/mol
(O2 é substância simples no estado padrão de entalpia)
H (reagentes) = -47 + 0 = -47
Produtos:
3 x CO2 (g) = 3 x (-94) = - 282 kcal/mol
4 x H2O (g) = 4 x (-68) = - 272 kcal/mol
H (produtos) = -282 - 272 = - 554 kcal/mol
Quarto passo: aplicar a fórmula
ΔH = H (dos produtos) - H (reagentes)
ΔH = - 554 - (- 47)
ΔH = - 554 + 47
ΔH = - 507 kcal/mol
Para esse método, é necessário que o problema ofereça a energia de ligação dos átomos. Para esse método, é importante relembrar um pouco da organização das moléculas através da geometria molecular. Para explicar melhor, vamos resolver a mesma equação do problema anterior, mas de outra forma. Calcule a variação de entalpia da seguinte equação: C3H8 (g) + O2 (g) -> CO2 (g) + H2O (l).
C - C --------------------- 80 kcal/mol
C - H ----------------------100 kcal/mol
O = O----------------------118 kcal/mol
H - O-----------------------110 kcal/mol
C = O-----------------------178 kcal/mol
Primeiro passo: balancear a equação
1 C3H8 (g) + 5 O2 (g) = 3 CO2 (g) + 4 H2O (l)
Segundo passo: ver a energia dos reagentes de acordo com a estrutura molecular.
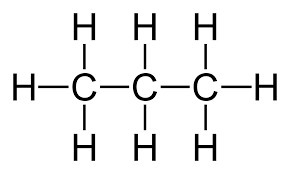
C3H8 (propano):
Na estrutura do propano, observamos que há duas ligações do tipo C - C. Se cada ligação C - C tem uma energia de 80 kcal/mol, então temos que: 2 x 80 = 160 kcal/mol. Como temos um mol de propano, 1x 2 x 80 = 160 kcal/mol. Ainda no propano, observamos oito ligações do tipo C - H. Se cada ligação C - H tem uma energia de 100 kcal/ mol, então temos que: 8 x 100 = 800 kcal/mol. Como temos um mol de propano, 1 x 8 x 100 = 800 kcal/mol. Assim, a energia total do propano é 960 kcal/mol.
Na estrutura do O2, temos apenas uma ligação dupla entre oxigênios, que vale 118 kcal/mol. Porém, temos 5 mol de oxigênio, por isso, fica: 5 x 1 x 118 = 590 kcal/mol, sendo essa a energia total do oxigênio.
O = O
A energia total dos reagentes, portanto, é 960 + 590 = 1550 kcal/mol
Terceiro passo: ver a energia dos produtos de acordo com a estrutura molecular.
CO2 (dióxido de carbono)
O = C = O
Na estrutura do CO2, percebemos a presença de duas ligações do tipo C = O, que tem uma energia de 178 kcal cada uma. Assim, 2 x 178 = 365. Como temos 3 mol de CO2, então: 3 x 2 x 178 = 1068 kcal/mol.
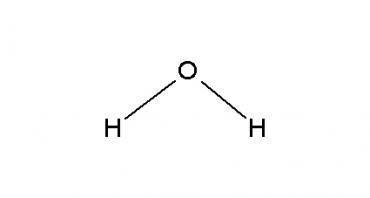
H2O (óxido de hidrogênio)
Nessa estrutura, percebemos a presença de duas ligações do tipo O - H. Cada uma dessas ligações tem uma energia de 110 kcal/mol. Assim, 2 x 110 = 220 kcal/mol. Como temos 4 mol de H2O, então temos que: 2 (ligações) x 4(mol) x 110 = 880 kcal/mol.
A energia total dos produtos, portanto, é 1068 + 880 = 1948 kcal/mol.
Quarto passo: determinar o sinal
Esse método se baseia no rompimento e formação de ligações. Onde as ligações são formadas e onde as ligações são rompidas?
No começo de uma reação, não existem produtos. Os átomos dos reagentes se rompem e, para isso, absorvem energia. Ou seja, os reagentes absorvem energia (têm sinal positivo, já que isso é um processo endotérmico). Já os produtos, à medida que a reação ocorre, são formados a partir dos átomos rompidos dos reagentes, em um processo que libera energia, ou seja, os produtos liberam a energia (têm sinal negativo, pois esse processo é exotérmico).
Isso nos leva a uma segunda fórmula:
ΔH = H rompida + H formada.
Quinto passo: aplicar a fórmula.
A energia total dos reagentes é + 1550 kcal/mol, sendo essa a energia das ligações que foram rompidas.
A energia total dos produtos é - 1948 kcal/mol, sendo essa a energia das ligações que foram formadas.
Assim, temos que:
ΔH = H rompida+ H formada
ΔH = + 1550 + (- 1948)
ΔH = + 1550 - 1948
ΔH = - 398 k cal
Assim, podemos saber, também, que esse processo é um processo exotérmico, mesmo que na faze de rompimento das ligações dos átomos dos reagentes haja um processo endotérmico.
- Lei de Hess
Esse método não possui uma fórmula, mas ele é um pouco mais complicado de ser feito. Iremos trabalhar com uma equação principal chamada "equação problema" e com outras equações. Vamos resolver um problema por esse método?
Calcular ΔH para a seguinte equação: C (gr) + H2 (g) -> C6H6.
Dados:
C (gr) + O2 (g) -> CO2 (g) ΔH1 = - 96 kcal/mol
H2 (g) + ½ O2 (g) -> H2O (l) ΔH2 = - 69 kcal/mol
C6H6 + 15/2 O2 (g) -> 6 CO2 (g) + 3 H2O (l) ΔH3= - 795 kcal/mol
Primeiro passo: balancear a equação problema.
6 C (gr) + 3 H2 (g) -> 1 C6H6.
Segundo passo: encontrar cada componente da equação problema nas equações dadas.
A equação problema é: C (gr) + H2 (g) -> C6H6. Por enquanto, vamos desconsiderar a quantidade de mol. Na primeira equação, temos:
C (gr) + O2 (g) -> CO2 (g)
Qual componente dessa equação também está presente na equação problema? A grafita, C (gr). Podemos marcar na equação problema.
Na segunda equação, temos:
H2 (g) + ½ O2 (g) -> H2O (l)
Qual componente nos interessa? O gás hidrogênio, H2, então, podemos marcar.
Na terceira equação temos:
C6H6 + 15/2 O2 (g) -> 6 CO2 (g) + 3 H2O
Qual componente nos interessa? O benzeno, C6H6, então, podemos marcar. Mas, espera aí, o benzeno da terceira equação não está do mesmo lado do benzeno da equação problema? Isso faz diferença? Temos que mudar? Sim, faz bastante diferença. Mas não é nada demais, podemos simplesmente inverter a terceira equação. Se antes era assim:
C6H6 + 15/2 O2 (g) -> 6 CO2 (g) + 3 H2O (l) ΔH3= - 795 kcal/mol
Agora ficou assim:
6 CO2 (g) + 3 H2O (l) -> C6H6 + 15/2 O2 (g) ) ΔH3= + 795 kcal/mol
Só cuide com o valor de ΔH; se a equação for invertida, o sinal também precisa ser invertido!
Terceiro passo: fazer alterações nas outras equações para chegar à equação principal.
Como fazemos isso?
Montamos um sistema, tal que:
I - C (gr) + O2 (g) -> CO2 (g) ΔH1 = - 96 kcal/mol
II - H2 (g) + ½ O2 (g) -> H2O (l) ΔH2 = - 69 kcal/mol
III - 6 CO2 (g) + 3 H2O (l) -> C6H6 + 15/2 O2 (g) ) ΔH3= + 795 kcal/mol
----------------------------------------------------------------------------------------------
6 C (gr) + 3 H2 (g) -> 1 C6H6 ΔH = ?
Temos algumas substâncias "intrusas" que não devem estar aí. Por isso vamos eliminá-las! Pense como se fosse uma equação matemática: se em ambos os lados os números forem positivos, ao "passar para o outro lado" teremos um número negativo. Se forem iguais, resulta em zero.
Vamos deixar em verde o que já está correto e não precisa de mudanças.
Nosso primeiro movimento já foi feito: inverter a equação III para que o benzeno ficasse do lado certo.
O que podemos fazer agora é multiplicar a equação I por seis; Já que, no final, precisaremos de seis mol de grafita. Assim:
I - 6 x C (gr) + 6 x O2 (g) -> 6 x CO2 (g) ΔH1 = - 96 kcal/mol x 6 = - 576 kcal/mol
II - H2 (g) + ½ O2 (g) -> H2O (l) ΔH2 = - 69 kcal/mol
III - 6 CO2 (g) + 3 H2O (l) -> C6H6 + 15/2 O2 (g) ) ΔH3= + 795 kcal/mol
Repare que qualquer alteração feita na equação afeta o ΔH da reação. Agora que temos a mesma quantidade de CO2 nos dois lados, podemos "cortar".
I - 6 C (gr) + 6O2 (g) -> 6 CO2 (g) ΔH1 = - 96 kcal/mol x 6 = - 576 kcal/mol
II - H2 (g) + ½ O2 (g) -> H2O (l) ΔH2 = - 69 kcal/mol
III - 6 CO2 (g) + 3 H2O (l) -> C6H6 + 15/2 O2 (g) ΔH3= + 795 kcal/mol
Precisamos de três mols de hidrogênio, portanto, multiplicamos a equação II por três. Ao fazer isso, também poderemos "cortar" a água.
I - 6C (gr) + 6O2 (g) -> 0 CO2 ΔH1 = - 96 kcal/mol x 6 = - 576 kcal/mol
II - 3 x H2 (g) + 3 x ½ O2 (g) -> 3 x H2O (l) ΔH2 = - 69 kcal/mol x 3 = -207 kcal/mol
III - 0 CO2 + 3 H2O (l) -> C6H6 + 15/2 O2 (g) ) ΔH3= + 795 kcal/mol
Agora que anulamos a água, podemos anular o oxigênio. Para o oxigênio, 3 x ½ (da equação 2) + 6 (da equação 1) = 7,5, da mesma forma que 15/2 = 7,5.
I - 6C (gr) + 6O2 (g) -> 0 CO2 ΔH1 = - 96 kcal/mol x 6 = - 576 kcal/mol
II - 3 H2 (g) + 3 x ½ O2 (g) -> 0 H2O (l) ΔH2 = - 69 kcal/mol x 3 = -207 kcal/mol
III - 0 CO2 + 0 H2O (l) -> C6H6 + 15/2 O2 (g) ΔH3= + 795 kcal/mol
Quarto passo: fazer a prova final, de forma que o sistema final seja:
I - 6C (gr) + 6O2 (g) -> 0 CO2 ΔH1 = - 96 kcal/mol x 6 = - 576 kcal/mol
II - 3 H2 (g) + 3 x ½ O2 (g) -> 0 H2O (l) ΔH2 = - 69 kcal/mol x 3 = -207 kcal/mol
III - 0 CO2 + 0 H2O (l) -> C6H6 + 15/2 O2 (g) ΔH3= + 795 kcal/mol
-----------------------------------------------------------------------------------------------------
6 C (gr) + 3 H2 (g) -> 1 C6H6
Quinto passo: somar as entalpias para achar a entalpia da equação problema.
ΔH = H1 + H2 + H3
ΔH = - 576 - 207 + 795
ΔH = + 12 kcal/mol
A termoquímica pode até parecer complicada, mas a maior parte dela é conceitos. Quanto aos cálculos, são compridos e (talvez) cansativos, mas não é nada que você não dê conta.
Texto por: Giovana Bagnara Luisi
Estudante de Química
Referências:
(TITO), Francisco Miragaia Peruzzo; CANTO, Eduardo Leite do. Química: na abordagem do cotidiano. 3. ed. São Paulo: Moderna, 2007. 760 p.
ATKINS, Peter; JONES, Loretta. Princípios de química: questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2012. 1026 p. Tradução técnica: Ricardo Bicca Alencastro.
Crédito das imagens:
https://www.google.com/url?sa=i&url=https%3A%2F%2Fwww.infoescola.com%2Fquimica%2Freacoes-endotermicas%2F&psig=AOvVaw0FZp-_r7qOY1AHzRRqNud2&ust=1589766153847000&source=images&cd=vfe&ved=0CAIQjRxqFwoTCJCSiMviuekCFQAAAAAdAAAAABAD
https://qph.fs.quoracdn.net/main-qimg-27d10bb7dc519c2760dc0ccf2288d77f.webp
https://s5.static.brasilescola.uol.com.br/img/2015/03/grafico-de-uma-reacao-exotermica.jpg
https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-energia-ativacao.htm
https://www.clipartmax.com/png/middle/177-1770213_file-h2o-2d-svg-chemical-structure-of-water.png
https://www.google.com/search?q=h2o+formula+molecular&tbm=isch&ved=2ahUKEwivtbL077vpAhVjA7kGHR6EDGEQ2-cCegQIABAA&oq=h2o+formula+molecular&gs_lcp=CgNpbWcQAzICCAAyBAgAEB46AggpOgQIABBDOgYIABAIEB5QhsMCWNLjAmCh6QJoAHAAeACAAaMBiAHvEpIBBDAuMTiYAQCgAQGqAQtnd3Mtd2l6LWltZw&sclient=img&ei=97DBXu_dHuOG5OUPnoiyiAY&bih=576&biw=1366&rlz=1C1NHXL_pt-BRBR805BR805#imgrc=kyTtirVqXiSU4M
