Isomeria
Essa parte é uma das mais importantes no estudo da Química. Veremos que os isômeros são as "antíteses" da nossa área. Há o bom e o mal. O cis e o trans. O que mata e o que cura.
Assim como irmãos gêmeos, os isômeros são, à primeira vista, praticamente iguais. Mas logo percebemos certas diferenças. Os isômeros são exatamente isso: compostos "irmãos gêmeos" que possuem uma pequena diferença sutil em sua fórmula estrutural.
Em termos mais técnicos, chamamos de isômeros compostos com a mesma fórmula molecular e fórmulas estruturais diferentes.
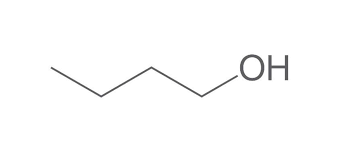
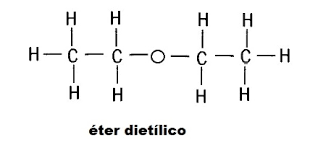
Um exemplo é o caso do butan-1-ol e do éter dietílico. Ambos têm fórmula de C4H10O, assim como ambos têm uma massa molar de 74 g/mol. Mas os pontos de fusão e ebulição são diferentes, e o mesmo ocorre com a densidade.
Para o butan-1-ol, o ponto de ebulição é -89°C, o de fusão é 118°C e a densidade é 0,81 g/cm^3.
Para o éter dietílico, o ponto de ebulição é 35°C, o de fusão é -116°C e a densidade é 0,71 g/cm^3.
É uma diferença significativa, exceto pela densidade. Mas por que isso acontece? Primeiramente, vamos comparar as fórmulas estruturais.
No butan-1-ol, o único oxigênio faz uma ligação com um carbono e um hidrogênio, enquanto no éter dietílico, o único oxigênio realiza duas ligações com dois carbonos. Como vimos em Termoquímica, as ligações C-O e O-H possuem diferentes energias. Isso afeta diretamente nos pontos de fusão e ebulição.
É comum, na Química Orgânica, um composto possuir mais de um isômero, e é o que muitas vezes acontece. O alcano C40H82 possui mais de 62 trilhões de isômeros, por exemplo.
Saiba mais: isomeria na Química Inorgânica.
Temos dois grandes tipos de isomeria: a espacial e a plana.
Isomeria plana
É aquela que apenas com uma boa observação da estrutura plana já conseguimos identificar alguma diferença. Ou seja, podemos "brincar" com a posição de inserção de um grupo de átomos de uma molécula. Por exemplo, podemos inserir um grupo -CH2 em uma molécula de C2H3 de dois modos diferentes, formando tanto o butano como o metilpropano.
Assim, é possível fazer uma classificação dos mesmos, em isômeros de função, tautomeria, isômeros de posição, metameria e isômeros de cadeia. Veremos com mais detalhes cada um deles.
Uma dica para classificar corretamente os isômeros planos é fazer uma sequência de perguntas: os compostos são da mesma função orgânica? Se não, há um equilíbrio entre eles? A cadeia carbônica é do mesmo tipo? Se não, a diferença está em um heteroátomo?
Isomeria de função
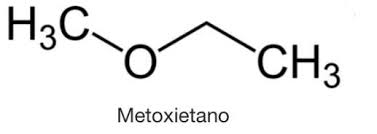
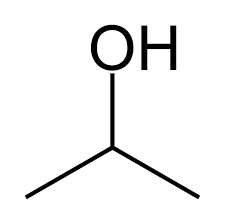
Observe as estruturas planas do metoxietano e do propan-2-ol.
A diferença entre eles está na função as quais pertencem. O propano-2-ol é um álcool, e o metoxietano é um éter. Pela nossa sequência de perguntas, diretamente reparamos que as funções orgânicas eram diferentes e que não havia um equilíbrio de coexistência entre os compostos, pois isso só ocorre com cetonas e enóis e aldeídos e enóis.
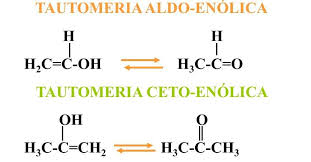
Tautomeria
É bem parecida com a isomeria de função. Mas, nesse caso, temos uma coexistência entre os isômeros, estabelecendo um equilíbrio químico entre a formação de um e a decomposição de outro. Ocorre principalmente com enóis e cetona e enóis e aldeídos. A tautomeria entre um enol e uma cetona é chamada de tautomeria cetoenólica, e a tautomeria entre um enol e um aldeído é chamada de tautomeria aldoenólica.
Esses isômeros recebem nomes especiais: tautômeros.
Na tautomeria aldoenóica, a ligação dupla entre carbonos é rompida para formar uma ligação dupla entre o oxigênio e o carbono. O hidrogênio do grupo hidroxila, no enol, se separa do oxigênio e se junta ao carbono, formando o grupo CH3. Repare que as ligações C=O e C-H permitem enquadrar esse composto como um aldeído.
Na tautomeria cetoenóica, há o rompimento da ligação dupla entre os carbonos e uma formação de uma ligação dupla com o oxigênio. O hidrogênio do grupo hidroxila, no enol, se desprende do oxigênio e se liga ao carbono para formar o grupo CH3. Repare que as ligações C=O e C-C permitem classificar esse composto como uma cetona.
Isomeria de cadeia
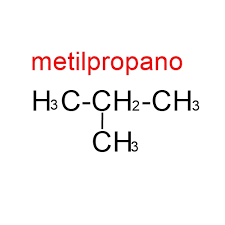
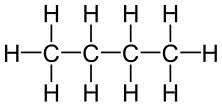
Vamos comparar, agora, o metilpropano e o butano, ambos com fórmula molecular de C4H10.
Ambos são hidrocarbonetos, então não são isômeros de função.
O metilpropano, entretanto, possui uma cadeia ramificada, um grupo metil ligado ao carbono central. Já o butano, por sua vez, possui uma cadeia linear, sem radicais.
Isomeria de posição
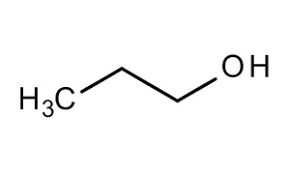
Observe o propano-1-ol e o propano-2-ol. Ambos são álcoois, ambos possuem fórmula molecular dada por C3H8O e ambos possuem cadeias ramificadas. O que os torna compostos diferentes?
A resposta é: o grupo hidroxila (OH). Observe que podemos trocar facilmente a posição desse grupo para obter compostos diferentes. Note que, aqui, não temos heteroátomos. No propan-1-ol, a hidroxila está ligada ao átomo de carbono no início da cadeia. Esse átomo, por sua vez, também está ligado a dois hidrogênios. As ligações presentes apenas nesse carbono ligado à hidroxila são:
- uma ligação O-H (na hidroxila),
- uma ligação C-O,
- duas ligações C-H,
- uma ligação C-C
No propan-2-ol, a hidroxila está ligada no átomo de carbono central. Esse átomo também se liga a dois átomos de carbono e a um átomo de hidrogênio. As ligações desse carbono central são:
- uma ligação O-H (na hidroxila),
- uma ligação C-O,
- uma ligação C-H,
- duas ligações C-C
Já sabemos que a diferença da quantidade de ligações interfere em vários aspectos de um composto.
Metameria
A metameria não deixa de ser um tipo de isomeria de posição. Só que ela está relacionada à posição de um heteroátomo dentro da cadeia carbônica. Observe o metoxipropano e o etoxietano.
Verificando as possibilidades de isomeria, vemos que ambos são éteres com cadeia linear e heterogênea, o que descarta as possibilidades de uma isomeria de função ou uma tautomeria e uma isomeria de cadeia.
A diferença está no átomo de oxigênio. No metoxipropano, o oxigênio está ligado ao primeiro e ao segundo carbono, enquanto no etoxietano o oxigênio está ligado ao segundo e terceiro carbono.
Repare que esses dois compostos são isômeros do butan-1-ol, apresentado no início do texto.
Isomeria espacial
A partir da estrutura plana dos compostos, fica difícil observar a diferença entre os isômeros. Nesses casos, é sempre bom contar com modelos 3-D para facilitar a compreensão, pois a conectividade das moléculas é a mesma, mas os átomos formam arranjos diferentes no espaço.
A isomeria espacial é dividida em isomeria geométrica e isomeria óptica.
Isomeria geométrica (ou cis-trans)
Observe a estrutura do brometo de etileno.
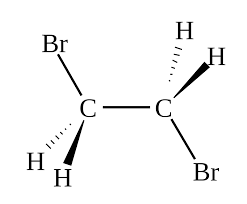
Se tivéssemos essa mesma molécula, só que em uma imagem na qual houvesse perfeita simetria entre os átomos, haveria diferencia? Seria um isômero?
Há, de fato, uma diferença, mas não é um isômero. A ligação simples entre carbonos permite uma rotação. Assim, os outros átomos giram ao redor dos carbonos, fazendo com que os carbonos girem em torno de si mesmos na horizontal. Esses compostos são chamados de conformações de uma mesma molécula.
A partir de agora, faremos um uso de um kit de modelos moleculares. Nas representações a seguir, cada cor representará um átomo. A fim de facilitar o entendimento e a fluidez do estudo, elaboramos uma pequena legenda.

Já no 1,2-dibromoeteno, a figura muda. Aqui, temos uma ligação dupla, que impede essa rotação. Pense como uma tábua solta pendurada por um prego: nesse caso, ela gira, mas se tiver dois pregos, isso não será possível. Com essa rotação interrompida, agora podemos dizer que esse composto possui um isômero.
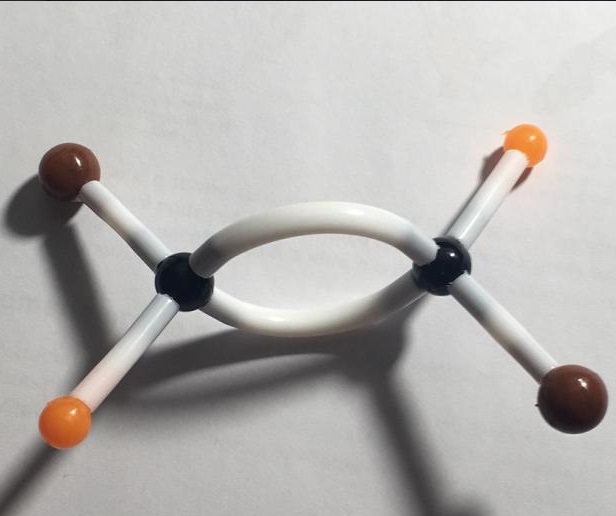
Os isômeros geométricos, também chamados de diastereoisômeros, se apresentam ou na forma cis ou na forma trans.
Quando considerarmos que os átomos ou grupos de átomos iguais de cada carbono estão de um mesmo lado do plano imaginário que corta a ligação dupla na horizontal, teremos um isômero cis.
Nesse caso, por exemplo, vamos considerar o bromo e o hidrogênio. Se os dois bromos estiverem "para cima", e os dois hidrogênios para baixo será o cis-1,2-dibromoeteno.
O isômero trans será aquele que tiver um carbono ligado a um átomo ou grupo voltado "para cima" e no outro carbono o mesmo grupo estará voltado "para baixo".
Condições para a ocorrência da isomeria geométrica:
- Em cadeia simples
Ligação dupla. Esse é o principal requisito. É um exemplo do que vemos acima. Como exemplo, temos os isômeros cis e trans do 1,2-dibromoeteno.
- Em cadeias cíclicas
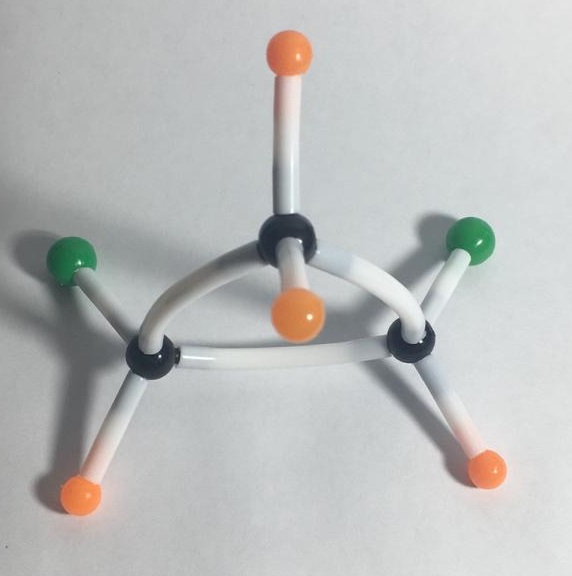
Nesse caso, a presença de saturação na cadeia é dispensada, pois o próprio formato cíclico funciona como o "segundo prego". Só é necessária a presença de dois átomos de carbonos ligados entre si e a ligantes diferentes. Como exemplo temos os isômeros do 1,2-diclorociclopropano.

E se os ligantes forem diferentes entre si? Não é problema. Apenas usamos outro sistema, já que a classificação cis-trans é usada para ligantes iguais.
O que tem que ser feito é olhar e anotar o número atômico de cada átomo ligado aos carbonos da ligação dupla. Isso facilita a visualização dos átomos de maiores números atômicos. Se esses átomos estiverem juntos, no mesmo lado do plano, será o Z e se estiverem um oposto ao outro, será o E.
Essa é uma molécula de 2-bromo-1-cloroprop-eno. Aqui, vamos fazer a mesma coisa: ver os números atômicos dos átomos ligados diretamente ao carbono que faz a ligação dupla.
Observe que temos um radical metila, em um carbono. Qual número atômico deve ser considerado? Apenas o do átomo ligado diretamente ao carbono que realiza ligação dupla. Não deve ser efetuada nenhuma soma ou algo do tipo.
Na primeira imagem, temos o carbono (Z=12) e o cloro (Z=17) do mesmo lado do plano imaginário, na parte de "cima", por assim dizer.
Na parte de baixo. temos o bromo (Z=35) e o hidrogênio (Z=1).
Os elementos com maiores números atômicos são o bromo e o cloro. Então, esse é o isômero E do 2-bromo-1-cloroprop-eno.
Isomeria óptica
O conceito da isomeria óptica se baseia nos espelhos. É como se colocássemos uma molécula em frente a ele. Ao serem sobrepostas, as imagens não são as mesmas, ou seja, temos um composto diferente, um isômero. Contudo, para isso, é necessário que a molécula seja assimétrica. Os isômeros ópticos são chamados de enantiômeros. Observe o CHBrClF.
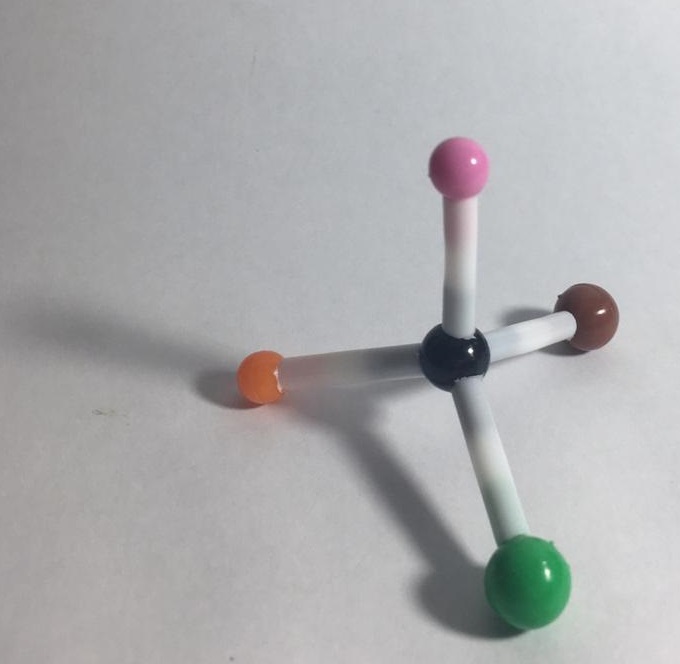
Quando fazemos a sobreposição da imagem real com a do espelho, obtemos compostos diferentes, portanto, eles são isômeros. Já se, ao realizar a sobreposição, os compostos forem iguais, não serão isômeros. Vamos ver: o metano possui um isômero óptico?

Não, pois o metano é uma molécula simétrica.
De fato, a assimetria é a condição suficiente para a existência dos enantiômeros. A assimetria acontece quando temos um carbono quiral.
O carbono é capaz de realizar quatro ligações; na isomeria, essa capacidade é aproveitada pois permite a quiralidade desse elemento. Ou seja: se um carbono realizar quatro ligações com quatro grupos ligantes diferentes, ele é classificado como quiral. Observe que, no primeiro exemplo, o carbono realiza ligações com o flúor, o hidrogênio, o bromo e o cloro.
Saiba mais: só o carbono é quiral?
Analisando a estrutura do CH3F, por exemplo, percebemos que não há quiralidade, pois dos quatro ligantes, três são hidrogênios. Quanto mais carbonos quirais houver, maior vai ser a quantidade possível de isômeros existentes.
Assim, o "reflexo" dessa molécula é igual a ela mesma; não é, portanto, um enantiômero.
Enantiômeros e a polarização da luz
Quando uma lâmpada emite luz, essas ondas luminosas vibram e propagam por vários planos de vibração, para a frente, para os lados, etc. Quando isso acontece, dizemos que temos uma luz não-polarizada. Ao passar por um polarizador, essa onda passa a vibrar em um único sentindo, sendo, então, a luz polarizada. Dois polarizadores alinhados permitem a passagem da luz, mas polarizadores perpendiculares dificultam e até mesmo impedem essa passagem.
Uma solução de enantiômeros, quando exposta à luz polarizada, provoca um desvio desse plano para a direita ou para a esquerda. Eles são, respectivamente, os enantiômeros dextrógiros e os enantiômeros levógiros. Quando temos esses dois enantiômeros em uma mesma quantidade em uma solução, essa solução é chamada de mistura racêmica.
Quando um feixe de luz polarizada passa por uma mistura com moléculas simétricas, não há desvio de luz, ou seja, são opticamente inativas. Isso também ocorre com misturas racêmicas, pois é como se os enantiômeros dextrógiros "anulassem" os levógiros, resultando em uma solução praticamente simétrica.
As propriedades físicas desses compostos são iguais, exceto no que diz respeito ao desvio do plano da luz. Quimicamente, suas propriedades são idênticas; exceto quando reagem com outros compostos quirais. Portanto, já que boa parte dos compostos orgânicos são quirais, a interação entre os enantiômeros e essas moléculas têm resultados bem diferentes, trazendo consequência para o organismo.
Saiba mais: enantiômeros e fármacos.
Texto por Giovana Bagnara Luisi
Estudante de Química
Referências:
(TITO), Francisco Miragaia Peruzzo; CANTO, Eduardo Leite do. Química: na abordagem do cotidiano. 3. ed. São Paulo: Moderna, 2007. 760 p.
ATKINS, Peter; JONES, Loretta. Princípios de química: questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman, 2012. 1026 p. Tradução técnica: Ricardo Bicca Alencastro.
SCARPELLINI, Carminella; ANDREATTA, Vinícius Barbosa. Manual compacto de Química: Ensino Médio. São Paulo: Editora Rideel, 2011. 448 p.
NAHAS, Matheus. Isômeros: os compostos distintos que apresentam a mesma fórmula molecular. São Paulo: Ftd, 2017. 31 v. (Sistema Marista de Educação).